診療・各部門
平成20年4月設置後、当センターでは、よりよい治療の提供ができるよう既存の治療法の評価を始め、エビデンスに基づいた新しい治療法の検討にも積極的に参加しております。
“チーム医療”の円滑化を目標に院内各部署との連携を取りながら、治験・臨床試験・臨床研究の実施体制作り(インフラ整備)を進めることが出来るよう努力しています。また、H21 年からは、医師主導型の臨床研究立案にも取り組み、登録医の先生方や近隣医療圏の先生方の協力を賜り、当院での治療評価・エビデンス(根拠ある)治療を目指しています。
各分野(医師・看護師・その他メディカルスタッフ)の臨床研究の支援を通して、院内スタッフが一丸となり、当院の理念の “良質で安全な医療の提供” ができるように努めていきたいと思います。 既に多くの薬や治療法がありますが、より個々の患者さまに合った 治療法があると思います。いわゆる難病などの治療薬が少ない病気や、 また、国外で承認済でも日本では承認されていないため保険適応外の薬など、まだまだ必要な薬や治療法があります。新GCP省令(医薬品の臨床試験の実施の基準に関する省令)により、近年、日本でも開発治験や臨床試験支援者(臨床研究コーディネーター:CRC)を配置する病院が増えています。CRCはより安全な医療の提供を心がけています。
自院設置の治験審査委員会を有しています
構成:医師3名、看護師1名、薬剤師1名、事務系2名、外部委員2名
体制
CRC(看護師) 1名
★地方の医療機関への治験依頼は、経済性および症例集積性の面などから、非常に減少しています。そこで、本来のCRC業務に加え、CRCの職能で業務できる分野の支援に積極的に取り組み、院内スタッフの臨床研究企画支援・統計解析支援を始め、地域の医療機関の方への臨床研究研修などを企画し参加を呼びかけています。
当院CRCの主な業務
① CRC業務
* 被験者スクリーニング対象症例の選定
(毎週1回カンファレンス:化学療法認定看護師・外来看護師・外来薬剤師・CRC)
* 被験者(患者様・家族)支援
同意説明、診察同席、治験スケジュール管理、服薬指導支援、問い合わせ窓口など
* 治験実施計画書(プロトコル)を遵守し治験規定項目の遂行(逸脱防止)
* 医師業務支援
症例報告書作成支援、重篤な有害事象報告書および医師作成の必須文書作成支援
* 製薬企業の対応
治験開始前から終了、および、治験薬承認までの種々の調整等
* 対象疾患毎の治験チームのインフラ整備
② 治験事務局業務
* 申請書類作成、製薬企業の対応、契約締結、経費
* 治験審査委員会運営
③ その他(研究支援)
* 院内教育研修企画
* 院外向け研修企画(計画立案、統計解析など基礎的内容を中心に研修)
* 院内主導の臨床研究の立案・統計解析支援
* 各種学会・研究会発表支援
* 臨床研究の研修企画・実施
CRCの位置付け
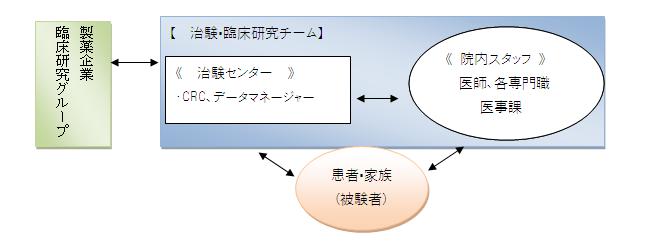
スタッフ 岩崎ユリ:CRC(看護師、日本SMO協会認定CRC)医学修士(バイオ統計学)
お問合せ先 TEL:0966-22-2191(内線 636)
e-mail:iwasaki-yuri@hitoyoshi.jcho.go.jp
臨床試験の新規登録、実施中の臨床試験の検索サイト
医学情報大学病院医療情報ネットワーク(UMIN)
臨床試験登録システム(UMIN-CTR)
http://www.umin.ac.jp/ctr/index-j.htm
(財)日本医薬情報センター(JAPIC)臨床試験情報
https://www.japic.or.jp/di/navi.php?cid=5
★教育サイト
ICR臨床研究入門(臨床研究に携わる方への教育サイト)
https://www.icrweb.jp/my/index.php